Läkemedelsnytt nummer 6 2026
Information från läkemedelscentrum.
Expeditionsintervall anges säkrast i dagar eller veckor
När du som förskrivare anger expeditionsintervall i dagar eller veckor vid en förskrivning säkerställer du att intervallet blir som du har tänkt dig. Det underlättar även för apoteksfarmaceuter vid hantering av förskrivningar med expeditionsintervall och minimerar riskerna för att patienter hämtar ut sina läkemedel för tidigt.
Skillnader mellan olika tidsmått påverkar hur expeditionsintervallet anges
Om expeditionsintervallet istället är angivet i tidsmåttet månader på en förskrivning visas inte automatiskt något uträknat datum till apoteken för nästa möjliga uttag. Det leder i sin tur till att spärren för expedition i apotekens datasystem uteblir, även om det är för tidigt att hämta ut läkemedlet. E-hälsomyndigheten (EHM) har istället valt att bygga in en varning som uppmanar apoteksfarmaceuten att själv räkna ut datum för nästa tillåtna expedition, baserat på den senaste expeditionen på förskrivningen.
Fördelaktigt att ange expeditionsintervall i dagar eller veckor
För expeditionsintervall som anges med tidsmåtten dagar respektive veckor visas ett exakt datum för nästa möjliga expedition automatiskt i apotekens system, och en spärr skapas för att hindra en expedition före det uträknade datumet. Tidsmått dagar och veckor väljs genom att expandera rullisten i utkorgen.
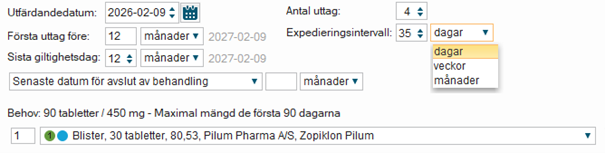
I utkorgen expanderas en rullist för att välja vilket tidsmått som expeditionsintervallet ska anges i på förskrivningen.
Bakgrund
Efter införandet av Nationella läkemedelslistan (NLL) har E-hälsomyndigheten (EHM) ändrat det datastöd som ges till apotek gällande expeditionsintervall. EHM anser att tidsmåttet månader är godtyckligt då antal dagar varierar mellan månaderna under året. Risken med att ange expeditionsintervall i månader blir därmed att patienten hämtar ut sitt läkemedel för tidigt.
Beslut om obesitasläkemedel skjuts upp
Tandvårds- och läkemedelsförmånsverket (TLV) utreder just nu om obesitasläkemedlet Wegovy (semaglutid) ska inkluderas i läkemedelsförmånerna. För närvarande är Wegovy inte subventionerat i Sverige, men läkemedlet går att hämta ut på apotek om patienten har ett giltigt recept. Förhandlingar om ett avtal mellan regionerna och läkemedelsföretaget pågår fortfarande. TLV väntar in resultatet av förhandlingen och kommer därför inte att fatta ett beslut om Wegovy ska ingå i läkemedelsförmånerna innan förhandlingarna är klara.
Merkostnadsersättning
En patient som har merkostnader till följd av en funktionsnedsättning kan i vissa fall få merkostnadsersättning. Försäkringskassan har nu förtydligat för regionerna vilka uppgifter ett läkarutlåtande om sådan ersättning för obesitasläkemedel behöver innehålla. Bland annat behöver det finnas en funktionsnedsättning i form av obesitas där Body Mass Index (BMI) är över 35 samt att funktionsnedsättningen ska antas bestå under minst ett år.
SBU-rapport - GLP-1-receptoragonister mot obesitas
Statens beredning för medicinsk och social utvärdering (SBU) har i en färsk rapport sammanfattat och kommenterat tre systematiska översikter från databasen Cochrane som alla utvärderar effekten av GLP-1-receptoragonister för behandling av obesitas. I rapporten konstateras att tirzepatid och semaglutid har en klinisk effekt på viktminskning jämfört med placebo. Däremot bedömer SBU att tillförlitligheten till resultaten är något lägre än vad översiktsförfattarna ansåg. SBU konstaterar att mer forskning behövs för att kunna bedöma om de tre läkemedlen semaglutid, liraglutid och tirzepatid är likvärdiga eller om något är mer effektivt än andra vid viktminskning.
Mer information
Allvarlig kvalitetsdefekt upptäckt i Arixtra förfylld spruta
Företaget som tillverkar Arixtra injektionsvätska i förfylld spruta har fått in rapporter om att en brun missfärgning och blockering förekommer i nålen på vissa sprutor. Denna kvalitetsdefekt är relaterad till förekomsten av en främmande järnpartikel som har oxiderat inuti nålen. Användning av en missfärgad spruta kan medföra risk för utebliven effekt på grund av blockering i nålen samt biverkningar om injektioner ges. Defekten uppskattas vara mycket sällsynt förekommande, men kan potentiellt finnas i alla Arixtra-produkter.
Vidta följande kontrollåtgärder innan du lämnar ut eller administrerar Arixtra
- Inspektera noggrant alla förfyllda sprutor för missfärgning vid kanylfattningen, det vill säga där nålen fäster vid sprutan.
- Om kanylfattningen i den förfyllda sprutan är missfärgad ska sprutan inte lämnas ut eller administreras. Defekta sprutor ska returneras till apoteksleverantör eller öppenvårdsapotek.
- Övriga kontrollåtgärder för Arixtra förfyllda sprutor återfinns i steg-för-steg-instruktionerna i produktens bipacksedel.
- Informera berörda patienter om att denna kvalitetsdefekt förekommer.
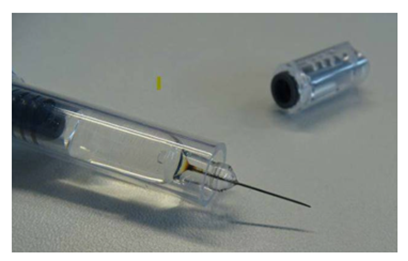
Exempel på spruta med missfärgning vid kanylfattningen.
Webbinarium om licens för läkemedel
Läkemedelsverket bjuder in till webbinarium om licens för läkemedel vid två tillfällen i mars. Webbinariet riktar sig i första hand till dig som är förskrivare och är ny inom området eller vill fräscha upp dina kunskaper om förskrivning av läkemedel via licens.
Tid och datum
- Tisdagen den 17 mars klockan 13.00–15.00
- Torsdagen den 19 mars klockan 9.00–11.00
Mer information och anmälan
Aktuella restnoteringar, utgående läkemedel och licensläkemedel
Här uppmärksammas ny information från restrådet. Uppdateringar görs löpande.
Denna vecka har vi inget nytt att informera om.
